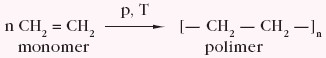Alkeny to węglowodory łańcuchowe, w cząsteczkach których występuje jedno wiązanie podwójne między atomami węgla, których walencyjne orbitale atomowe są w stanie hybrydyzacji sp2. Te dwa atomy węgla oraz cztery atomy bezpośrednio związane z nimi leżą w jednej płaszczyźnie.
Długość wiązania podwójnego 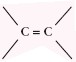 jest krótsza od długości wiązania pojedynczego i wynosi 134 pm, ale energia wiązania jest większa i wynosi 682 kJ/mol.
jest krótsza od długości wiązania pojedynczego i wynosi 134 pm, ale energia wiązania jest większa i wynosi 682 kJ/mol.
Pamiętając, że na wiązanie podwójne składa się jedno wiązanie mocne σ i drugie słabsze π wnioskujemy, że wiązanie π będzie łatwo ulegać rozerwaniu podczas reakcji chemicznej. Ten fakt decyduje o dużej aktywności chemicznej alkenów.
Alkeny tworzą szereg homologiczny o wzorze CnH2n. W szeregu homologicznym łańcuchowych alkenów ze wzrostem liczby atomów węgla:
- zmienia się stan skupienia,
- rosną temperatury topnienia i wrzenia.
Poniżej podano wzory i nazwy wybranych węglowodorów:
CH3-CH=CH-CH(CH3)CH2-CH3 4-metyloheks-2-en
CH2=C(C2H5)-CH2-CH2-CH3 2-etylopent-1-en
Charakterystyczną cechą alkenów jest zdolność do reakcji addycji i reakcji polimeryzacji. Addycją nazywa się proces przyłączania do atomów węgla połączonych wiązaniem podwójnym lub potrójnym cząsteczek homo- lub heteroatomowych, w wyniku czego zmniejsza się krotność wiązania. Reakcja addycji zachodzi wtedy, gdy dwa substraty łączą się ze sobą tworząc jeden produkt. Polimeryzacja to reakcja, w której związek wielkocząsteczkowy (polimer) tworzy się z pojedynczych cząsteczek związku o małej masie cząsteczkowej (monomer) bez wydzielania produktów ubocznych. Procesem odwrotnym do polimeryzacji jest depolimeryzacja.
Reaktywne miejsca w cząsteczce alkenu:
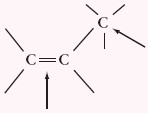
Alkeny jako węglowodory nienasycone mogą przyłączać:
- cząsteczkę wodoru:
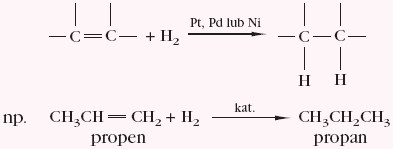
- cząsteczkę halogenu X2 (środowisko CCl4):
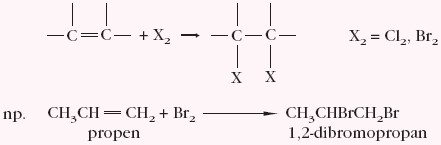
- cząsteczkę halogenowodoru HX:
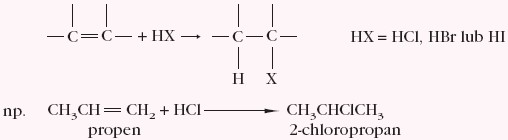
Addycja cząsteczki heteroatomowej HX zachodzi zgodnie z regułą Markownikowa, która mówi, że atom wodoru w reakcji addycji przyłącza się do atomu węgla związanego z większą liczbą atomów wodoru, czyli mniej podstawionego. - cząsteczkę wody (hydratacja):
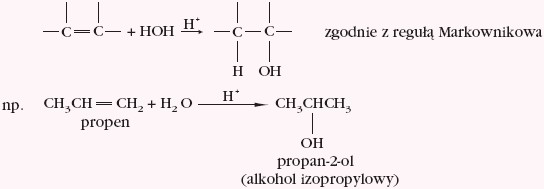
Potwierdzeniem charakteru nienasyconego związku jest pozytywny wynik w reakcjach z wodą bromową i roztworem manganianu(VII) potasu. Podczas reakcji alkenu z manganianem(VII) potasu tworzą się diole, np.
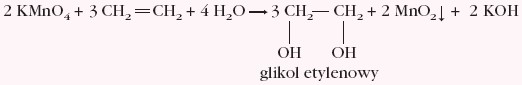
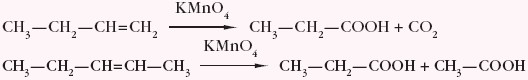
W środowisku kwaśnym lub obojętnym z niewielką wydajnością może zachodzić proces utleniania alkenu pod wpływem KMnO4 do kwasu karboksylowego i CO2 lub mieszaniny kwasów karboksylowych, co przedstawiono poniższym schematem:
W odpowiednich warunkach (temperatura, ciśnienie, katalizator) ulegają reakcji polimeryzacji: