Układ utworzony przez połączenie dwóch elektrod za pomocą klucza elektrolitycznego nosi nazwę ogniwa elektrochemicznego. W ogniwie elektrody połączone są ze sobą przewodnikiem metalicznym, który pełni rolę przekaźnika elektronów, a roztwory kluczem elektrolitycznym, który umożliwia przepływ niewielkiej liczby jonów, wyrównujący bilans ładunku. Zamknięcie obwodu np. amperomierzem, woltomierzem spowoduje, że ich wskazówka wychyli się, czyli w układzie płynie prąd. Ogniwo jest źródłem prądu na skutek samorzutnego przebiegu w nim reakcji utleniania-redukcji.
W ogniwie są dwie elektrody:
- na jednej następuje wydzielanie metalu, czyli zachodzi redukcja – KATODA
Me Iz+ + ze– → Me I - na drugiej jony metalu przechodzą do roztworu, czyli zachodzi utlenianie – ANODA
Me II → Me IIz+ + ze–
Elektroda o niższej wartości potencjału jest anodą, a wyższej – katodą. Katoda ma znak dodatni, a anoda ujemny. Elektrony płyną od anody do katody.
Sumaryczna reakcja zachodząca w ogniwie:
Me Iz+ + Me II → Me I + Me IIz+
Siła elektromotoryczna SEM powstałego ogniwa będzie równa różnicy potencjałów elektrod (od potencjału katody odejmuje się potencjał anody):
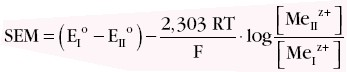
Ogniwo Daniella:

Sumaryczna reakcja przebiegająca w ogniwie:
Zn + Cu2+ → Zn2+ + Cu
Co się dzieje podczas pracy ogniwa?
- na płytce cynkowej gromadzą się elektrony, które przez przewodnik biegną do elektrody miedziowej – atomy cynku przechodzą do roztworu w postaci kationów (elektroda cynkowa roztwarza się),
- elektroda miedziowa oddaje płynące do niej przez przewód elektrony (od elektrody cynkowej) jonom miedzi znajdującym się w sąsiedztwie elektrody. Na tej elektrodzie osadza się metaliczna miedź.
Ogniwo pracuje, czyli prąd płynie, dopóki nie nastąpi całkowite roztworzenie płytki cynkowej lub redukcja wszystkich kationów miedzi Cu2+.

