Stężenie roztworu to stosunek ilości substancji rozpuszczonej do określonej ilości (objętości lub masy) roztworu.
Stężenie procentowe Cp wyraża liczbę gramów substancji rozpuszczonej znajdującej się w 100 gramach roztworu:
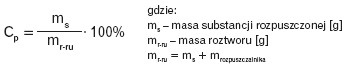
Stężenie molowe Cm określa liczbę moli substancji rozpuszczonej w 1 dm3 (1000 cm3)roztworu. Jednostką stężenia molowego jest mol/dm3.

Stężenie procentowe można łatwo przeliczyć na stężenie molowe (i odwrotnie), jeśli zna się wartość gęstości roztworu. Wzór na stężenie procentowe ma następującą postać:
![]()
Masę substancji rozpuszczonej (ms) i masę roztworu (mr–ru) można zapisać przy pomocy równań:
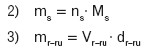
Podstawiając do równania 1 równania 2 i 3 otrzymuje się:
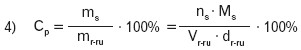
Wiemy, że przekształcając wzór na stężenie molowe (Cm), objętość roztworu można zapisać jako:
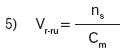
Podstawiając do równania 4 równanie 5 otrzymuje się:
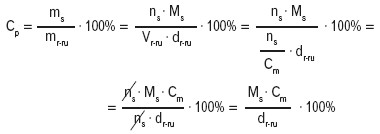
Przeliczenia stężenia procentowego na molowe (i odwrotnie) można dokonać, używając poniższych równań, pamiętając przy tym, że gęstość musi być wyrażona w g/dm3.

Co zawiera 200 cm3 wodnego roztworu HCl o stężeniu 30% i gęstości 1,14 g/cm3?
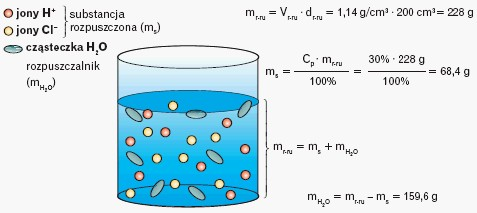
Przygotowując roztwór o określonym stężeniu molowym i określonej objętości należy:
- obliczyć liczbę gramów substancji rozpuszczanej potrzebną do sporządzenia roztworu, a następnie odważyć tę ilość substancji,
- do kolby o określonej objętości miarowej wlać trochę rozpuszczalnika, a następnie wsypać (ilościowo przenieść) odważoną ilość substancji rozpuszczanej,
- po rozpuszczeniu substancji dopełnić kolbę rozpuszczalnikiem do określonej objętości (czyli do tzw. kreski),
- całość dokładnie wymieszać.

