Ważnym homologiem benzenu jest metylobenzen zwany zwyczajowo toluenem. Jego właściwości chemiczne przedstawiono poniżej.
- Toluen w obecności silnego utleniacza, np. KMnO4, tworzy kwas benzoesowy, co przedstawiono poniżej ogólnym schematem:
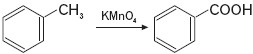
- Toluen w określonych warunkach (katalizator) ulega uwodornieniu:
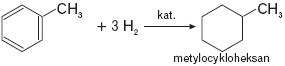
Poniżej przedstawiono schematy obrazujące sposób otrzymywania toluenu oraz jego wybrane właściwości chemiczne.
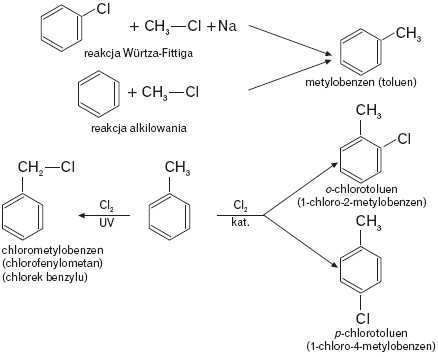
Grupa –CH3 zaliczana jest do podstawników I rodzaju i stąd w reakcjach opisanych powyżej otrzymuje się mieszaninę związków: pochodną orto i para.
Toluen poddany nitrowaniu (na zimno wobec mieszaniny nitrującej) daje 2,4,6-trinitrotoluen,stosowany jako materiał wybuchowy (trotyl, TNT).
Toluen jest bezbarwną, palną cieczą o charakterystycznym zapachu, nierozpuszczalną w wodzie, ale łatwo mieszającą się z rozpuszczalnikami organicznymi, np. etanolem, eterem czy benzenem. Toluen jest stosowany w przemyśle do produkcji tworzyw sztucznych, farb, lakierów i materiałów wybuchowych, jest także składnikiem paliw lotniczych. W laboratoriach chemicznych toluen stosowany jest jako rozpuszczalnik oraz substrat w syntezach organicznych.
Zastąpienie dwóch atomów wodoru w cząsteczce benzenu grupami metylowymi prowadzi do uzyskania trzech izomerycznych dimetylobenzenów, czyli ksylenów.
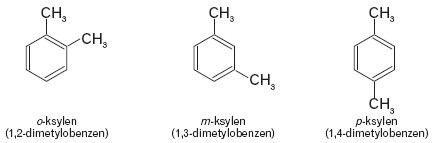
Istnieją również węglowodory aromatyczne o pierścieniach skondensowanych, np. naftalen, antracen i fenantren.
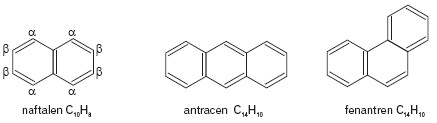
Korzystając z reguły Hückla stwierdza się, że w cząsteczce naftalenu jest dziesięć zdelokalizowanych elektronów π.
Jako związek aromatyczny naftalen ulega np. nitrowaniu. W cząsteczce naftalenu– w przeciwieństwie do benzenu – atomy wodoru nie są równocenne. Wprowadzenie pierwszego podstawnika pozwala na otrzymanie dwóch izomerycznych mononitropochodnych, co przedstawia poniższy schemat.
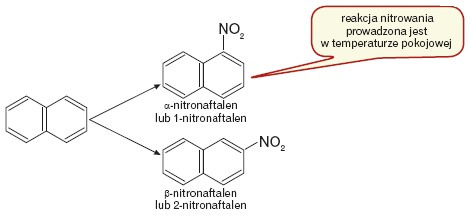
Rodzaj produktu zależy od warunków nitrowania, np. temperatury. Zazwyczaj w temperaturze pokojowej i nieco wyższej jako główny produkt powstaje izomer α.

