| tlenowe, np. H2CO3, H3PO4 | beztlenowe, np. HCl |
| jednoprotonowe, np. HNO2 | wieloprotonowe, np. H2SO4 |
| silnie utleniające (utleniaczem są atomy NV, SVI), np. kwas azotowy(V), stężony kwas siarkowy(VI) | słabo utleniające (utleniaczem są atomy HI), np. HCl |
| trwałe, np. H2SO4, HNO3, H3PO4 | nietrwałe, np. H2CO3, H2SO3, HNO2 |
| elektrolity mocne, np. HCl, HBr, HI,H2SO4, HNO3 | elektrolity słabe, np. H2S, HF, HClO |
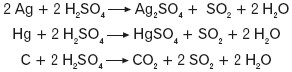
Z kwasami silnie utleniającymi reagują zarówno metale, jak i niemetale, np.:
Niektóre metale, np. cynk, w specyficzny sposób reagują ze stężonym kwasem azotowym(V). W określonych warunkach powstają następujące produkty:
![]()
Z kwasami słabo utleniającymi reagują metale znajdujące się w szeregu napięciowym przed wodorem (ujemne standardowe potencjały elektrod) wypierając z kwasów wodór. Metale znajdujące się w szeregu napięciowym za wodorem (dodatnie standardowe potencjały elektrod) nie reagują – w temperaturze pokojowej – z tymi kwasami, np.:
![]()
Specyficzną mieszaninę kwasów tworzy tzw. woda królewska, czyli mieszanina stężonych kwasów HCl i HNO3 w stosunku objętościowym 3:1. Złoto jako metal szlachetny rozpuszcza się dopiero w wodzie królewskiej.
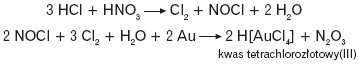
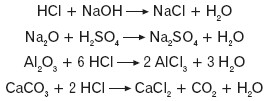
Kwasy reagują z zasadami, tlenkami zasadowymi i amfoterycznymi, solami kwasów słabszych i bardziej lotnych oraz – o czym sygnalizowano powyżej – z metalami.