Chlorowcokwasy wykazują wszystkie typowe właściwości wynikające z obecności grupy karboksylowej i atomu chlorowca w reszcie węglowodorowej:
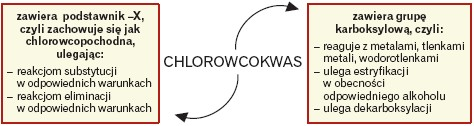
Inne swoiste właściwości są wynikiem współdziałania grupy –COOH i atomu –X i stanowią podstawę do omówienia właściwości chlorowcokwasów w zależności od usytuowania atomu –X względem grupy karboksylowej. Ponieważ najczęściej mamy do czynienia z chlorokwasami, na ich podstawie zostaną omówione te właściwości:
a) α-chlorokwasy w reakcji z mocną zasadą w środowisku wodnym tworzą odpowiednieα-hydroksykwasy, np.:
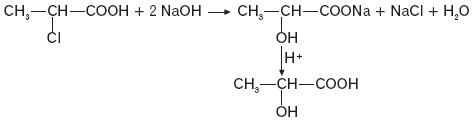
α-chlorokwasy pod wpływem nadmiaru amoniaku tworzą odpowiednie α-aminokwasy, np.:
![]()
α-chlorokwasy w reakcji z mocną zasadą w środowisku alkoholowym ulegają eliminacji, tworząc α, β-nienasycone kwasy, np.:
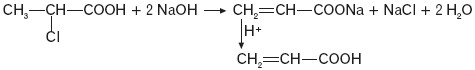
b) β-chlorokwasy w reakcji z mocną zasadą w środowisku alkoholowym ulegają eliminacji, tworząc α, β-nienasycone kwasy, np.:
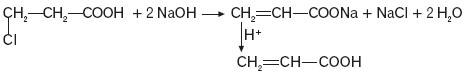
Poniższa tabela przedstawia wartości stałych dysocjacji wybranych kwasów karboksylowych.
| wzór wybranego kwasu | stała dysocjacji Ka |
| CH3COOH | 1,8 · 10–5 |
| CH2Cl--COOH | 1,4 · 10–3 |
| CHCl2--COOH | 6,3 · 10–2 |
| CCl3--COOH | 2,5 · 10–1 |
| CF3--COOH | 5,0 · 10–1 |
Analiza m.in. tych danych pozwala na wyciągnięcie następujących wniosków:
| czynnik | sposób, w jaki dany czynnik wpływa na zmianę mocy kwasu |
| rodzaj podstawnika | im bardziej elektroujemny podstawnik, tym większa moc kwasu |
| położenie podstawnika | im bliżej grupy karboksylowej znajduje się podstawnik ,tym większa moc kwasu |
| liczba podstawników | im więcej podstawników, tym większa moc kwasu |
Na przykład:
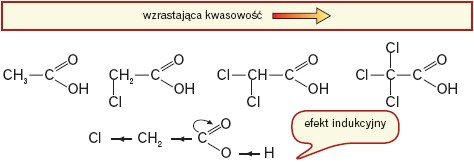
Obecność atomu chlorowca (podstawnik o dużej elektroujemności) wywołuje efekt indukcyjny (przesunięcie gęstości elektronowej ku podstawnikowi), który zwiększa deficyt elektronowy na atomie węgla grupy karboksylowej, a tym samym osłabia wiązanie O–H w grupie karboksylowej. Skutkiem tego jest zwiększona moc kwasu. Ponieważ efekt indukcyjny chlorowca związany jest z jego elektroujemnością, najsilniej zdysocjowane są chlorokwasy, a słabiej bromokwasy. Należy pamiętać, że efekt ten maleje wraz z oddalaniem się chlorowca od grupy karboksylowej. Zatem: moc kwasu jest tym większa, im bardziej elektroujemny jest podstawnik X, więcej jest atomów X i im one są bliżej grupy karboksylowej.

