Estry ulegają hydrolizie, która zachodzi zarówno w środowisku kwaśnym, jak i zasadowym.
![]()
Hydroliza w środowisku kwaśnym jest procesem odwracalnym.
![]()
Hydroliza w środowisku zasadowym jest praktycznie nieodwracalna.
Estry ulegają reakcji alkoholizy (transestryfikacji) oraz amonolizy, np.:
Alkoholiza, czyli reakcja estru z alkoholem prowadząca do otrzymania nowego estru i alkoholu, jest reakcją odwracalną zarówno w środowisku kwaśnym, jak i zasadowym.
![]()
Amonoliza, czyli reakcja estru z amoniakiem, prowadzi do otrzymania amidu i alkoholu.
![]()
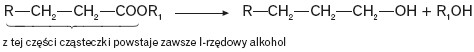
W odpowiednich warunkach możliwa jest redukcja estru, co przedstawiono na ogólnym schemacie:
Estry mogą pochodzić również od kwasów nieorganicznych, np. kwasu siarkowego(VI), kwasu azotowego(V) i kwasu fosforowego(V), np.:
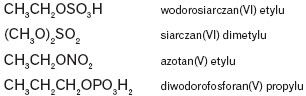
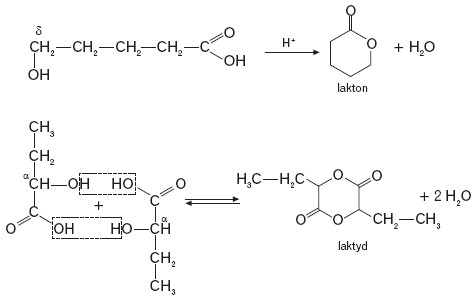
Istnieją cykliczne estry, które otrzymać można w trakcie wewnątrzcząsteczkowej estryfikacji γ- lub δ-hydroksykwasów (laktony) oraz w procesie kondensacji dwóch cząsteczek α-hydroksykwasu (laktydy), np.: