Chrom na powietrzu pokrywa się warstewką tlenku chromu(III) – jest to pasywacja. Wskutek obecności ochronnej warstewki tlenku, chrom nie reaguje z wodą,mimo że jest metalem o ujemnym potencjale elektrochemicznym. W reakcji z kwasem solnym i rozcieńczonym siarkowym(VI) tworzy – obok wydzielonego wodoru– związki na II stopniu utlenienia (warunki beztlenowe) lub III stopniu utlenienia (warunki tlenowe):
![]()
Chrom pod wpływem stężonego kwasu azotowego(V) i siarkowego(VI) ulega pasywacji.
W temperaturze czerwonego żaru chrom reaguje z parą wodną.
![]()
Powstały tlenek chromu(III) Cr2O3 obok tlenku chromu(II) CrO i tlenku chromu(VI) CrO3 stanowi jeden z trzech podstawowych tlenków chromu. Ich charakter chemiczny zmienia się ze zmianą stopnia utlenienia chromu:

Tlenek chromu(II) – substancja o barwie czarnej – reaguje z kwasami, np.:
![]()
Tlenek ten po ogrzaniu w obecności tlenu rozżarza się i przechodzi w tlenek chromu(III):
![]()
Roztwory wodne rozpuszczalnych soli chromu(II) są niebieskie, a soli chromu(III) – szarozielone.
Tlenek chromu(III) – szarozielona substancja – posiada właściwości amfoteryczne. Potwierdzają to poniższe równania reakcji:
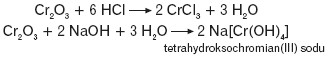
Tlenek ten powstaje podczas termicznego rozkładu wodorotlenku chromu(III):
![]()
Tlenek chromu(VI) – pomarańczowo-czerwona substancja o charakterze kwasowym, reaguje z wodą, tworząc silny, istniejący tylko w roztworze kwas chromowy(VI):
![]()
Zakwaszenie tego roztworu powoduje utworzenie szeregu kwasów polichromowych(VI), z których najważniejszy to kwas dichromowy(VI) H2Cr2O7, również istniejący tylko w roztworze wodnym.
Sole najważniejszych kwasów chromowych to odpowiednio: chromiany(VI) – barwa żółta – i dichromiany(VI) – barwa pomarańczowa, które można otrzymać w następujących reakcjach:
![]()
Chromian(VI) w środowisku kwaśnym jest związkiem nietrwałym i przekształca się w pomarańczowy dichromian(VI):
![]()
Dichromian(VI) w środowisku zasadowym jest związkiem nietrwałym i przekształca się w żółty chromian(VI).
![]()
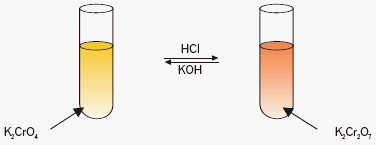
Podsumowując można stwierdzić, że w roztworze wodnym obserwuje się zależność występowania jonów chromianowych(VI) i dichromianowych(VI) od pH roztworu.
Chromiany(VI) i dichromiany(VI) posiadają właściwości utleniające, np.:
![]()
Mieszanina stężonego H2SO4 i K2Cr2O7 jest nazywana chromianką. Ma silne właściwości utleniające i stosowana jest nadal (mimo trującego charakteru) do czyszczenia naczyń laboratoryjnych.
Niektóre sole chromu ulegają termicznemu rozkładowi, np.:
![]()
Doświadczenie to nosi nazwę „wulkanu chemicznego”.
Chrom tworzy dwa wodorotlenki. Wodorotlenek chromu(II) – ciemnobrunatna substancja – posiada właściwości zasadowe, czyli reaguje z kwasami, np.:
![]()
Wodorotlenek chromu(III) to szarozielony, galaretowaty osad o właściwościach amfoterycznych. Wytrąca się z roztworów soli chromu(III) pod wpływem amoniaku,np.:
![]()
Właściwości amfoteryczne Cr(OH)3 potwierdzają równania:
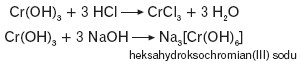
Właściwości utleniająco-redukujące związków chromu zmieniają się ze zmianą stopnia utlenienia chromu w danym związku:
- związki chromu(II) są reduktorami,
- związki chromu(III) w zależności od doboru pozostałych substratów mogą pełnić rolę zarówno utleniacza, jak i reduktora,
- związki chromu(VI) są utleniaczami.

