1. Występowanie wody w przyrodzie:
a) woda = 2/3 powierzchni Ziemi; 90% wody słone
b) woda w przyrodzie:
- lodowce
-chmury
-zbiorniki wodne
- organizmy żywe
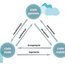
c) obieg wody w przyrodzie:
Woda w postaci opadów zasila rzeki, morza, oceany, wnika w glebę, jest pobierana przez organizmy żywe; dzięki parowaniu z gleby, zbiorników wodnych i organizmów żywych woda przedostaje się do atmosfery, dzięki czemu obieg się zamyka.
c) woda w 3- ech stanach skupienia:
ciecz – gaz (parowanie)
gaz – ciecz (skraplanie)
ciecz – stały (krzepnięcie)
stały – ciecz (topnienie)
gaz – stały (resublimacja)
stały – gaz (sublimacja)
2. Zmiana objętości i gęstości wody:
- woda największą gęstość ma w temperaturze 4* C
- gęstość wody w 4* C = 1 g/cm3
- w stanie gazowym woda ma gęstość najmniejszą, a objętość największą.
2. Skale temperatur:
a) Celsjusza 1*C
b) Kelwina 1K
c) Fahrenheita 32*F
3. Budowa cząsteczki wody:
Substancje, które rozpuszczają się w :
a) wodzie : cukier, sól, alkohol, atrament, sok, ocet, denaturat;
b) benzynie : plastik, klej, żywica.
Dlaczego woda jest tak ważna na Ziemi?
Ponieważ bez wody nie istniałoby życie.
Wyjaśnij co to znaczy, że H2O ma budowę polarną?
Elektrony przesuwają się w jedną stronę tej cząsteczki, a protony w drugą stronę.
Dlaczego woda nie dla wszystkich substancji jest dobrym rozpuszczalnikiem?
Ponieważ woda ma budowę polarną, a cząsteczka posiadająca taką właśnie budowę może rozpuszczać tylko cząsteczki o takiej samej budowie.
Dlaczego woda raz wrze w temperaturze 95*C, a raz w 100*C?
Gdy ciśnienie zewnętrzna jest inne, zmieniają się temperatury wrzenia i topnienia.
4. Podział substancji ze względu na rozpuszczalność w wodzie:
a) rozpuszczalne: cukier, sól, alkohol, kryształki siarczanu (VI) miedzi (II)
b) nierozpuszczalne: żywica, plastik, piasek
5. Czynniki wpływające na prędkość rozpuszczania substancji:
a) ciecz – ciało stałe ( lub ciecz ) – temperatura, mieszanie, rozdrobnienie, ilość, rodzaj substancji rozpuszczanej, rodzaj rozpuszczalnika;
b) ciecz – gaz – temperatura ( czym wyższa temperatura tym mniejsza rozpuszczalność ), im wyższe ciśnienie tym większa rozpuszczalność.
6. Roztwór – mieszanina co najmniej 2-óch składników, substancji rozpuszczonej i rozpuszczalnika.
Podział roztworów w zależności od rodzaju substancji rozpuszczonej i rozpuszczalnika:
- stałe ( stopy metali: stal, duraluminium, brąz, mosiądz )
- ciekłe ( ocet i woda, alkohol i woda )
- gazowe ( powietrze )
Podział roztworów ze względu na wielkość cząsteczek substancji rozpuszczonej:
- właściwy ( mniejsze niż 10-9m )
- koloid ( od 10-9m do 10-7m )
- zawiesina ( od 10-6 m do 10-5m )
Podział roztwór ze względu na ilość substancji rozpuszczonej:
- nasycony
- nienasycony ( stężony lub rozcieńczony )
Roztwór nasycony – to taki roztwór, w którym nie da się rozpuścić więcej substancji w danej temperaturze.
Roztwór nienasycony – to roztwór, w którym w danej temperaturze można jeszcze rozpuścić pewną ilość danej substancji.
Rozpuszczalność – to liczba gramów substancji, którą można rozpuścić w 100g rozpuszczalnika w danej temperaturze przy stałym ciśnieniu.
Efekt Tyndala – to rozproszenie światła przechodzącego przez układ koloidalny, w skutek ugięcia się promieni na cząsteczkach fazy rozproszonej.
7. Jak z nasyconego uzyskać r. nienasycony i odwrotnie?
r. nasycony – r. nienasycony : ogrzać, + rozpuszczalnik
r. nienasycony – r. nasycony : odparować rozpuszczalnik, + substancji rozpuszczanej, ochłodzić
8.
5% roztwór = 5g sub - 100g roztworu
0,1% roztwór = 0,1 g syb – 100g roztworu
Opracowania powiązane z tekstem
Treść zweryfikowana i sprawdzona
Zgodnie z misją, Redakcja serwisu dokłada wszelkich starań, aby dostarczać rzetelne i sprawdzone treści edukacyjne.
Dodatkowe oznaczenie "Sprawdzona treść" wskazuje, że dany materiał został zweryfikowany przez Redakcję lub ekspertów współpracujących z serwisem.
Weryfikacja tekstu odbywa się na następujących poziomach:
1. Sprawdzenie tekstu pod kątem ewentualnych błędów ortograficznych, stylistycznych, interpunkcyjnych lub innych.
2. Weryfikacja tekstu pod kątem błędów rzeczowych.
3. Sprawdzenie materiału pod kątem ich aktualności.
Dodatkowe oznaczenie "Sprawdzona treść" wskazuje, że dany materiał został zweryfikowany przez Redakcję lub ekspertów współpracujących z serwisem.
Weryfikacja tekstu odbywa się na następujących poziomach:
1. Sprawdzenie tekstu pod kątem ewentualnych błędów ortograficznych, stylistycznych, interpunkcyjnych lub innych.
2. Weryfikacja tekstu pod kątem błędów rzeczowych.
3. Sprawdzenie materiału pod kątem ich aktualności.