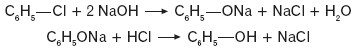
Fenol otrzymuje się w reakcjach opisanych poniższymi równaniami:
Można go również otrzymać podczas hydrolizy kwasów sulfonowych, zachodzącej w środowisku zasadowym w podwyższonej temperaturze:
![]()
Fenol wykazuje wyraźny charakter kwasowy. W roztworze wodnym dysocjuje jak kwas, czyli odszczepia kation wodoru H+ (uproszczony zapis):
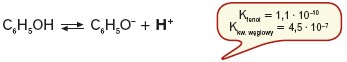
Fenol zaliczany jest do słabych kwasów.
Kwas węglowy jako mocniejszy kwas wypiera słabszy kwas, czyli fenol z jego soli:
![]()
Fenol reaguje z metalami aktywnymi (litowce) i mocnymi zasadami:
![]()
Fenolan potasu jako sól słabego kwasu i mocnej zasady ulega hydrolizie anionowej. Wodny roztwór tego związku posiada odczyn zasadowy, co potwierdza poniższy zapis tego procesu.
![]()
Reakcją charakterystyczną na wykrywanie fenolu jest reakcja z solami żelaza(III), w której tworzą się związki zabarwiające roztwór na kolor fioletowy, granatowy lub czerwony. Powstające fenolany żelaza(III) mają charakter związków koordynacyjnych.
Fenol jest związkiem aromatycznym i stąd ulega również reakcjom charakterystycznym dla tych związków, np. bromowaniu i nitrowaniu. Reakcje te zachodzą dużo łatwiej niż w przypadku benzenu.
a) bromowanie (bez katalizatora) – powstaje 2,4,6-tribromofenol
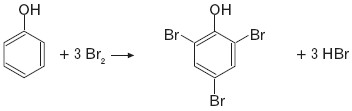
b) nitrowanie (rozcieńczony HNO3) – powstaje mieszanina o-nitrofenolu i p-nitrofenolu (schemat)
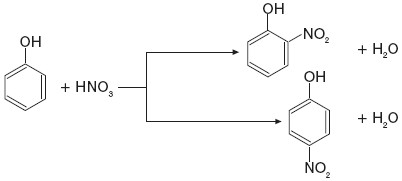
Grupa –OH w cząsteczce fenolu, jako podstawnik I rodzaju, kieruje następny podstawnik w pozycje orto i para.
Poniżej przedstawiono schemat przemian chemicznych, w których fenol jest substratem.
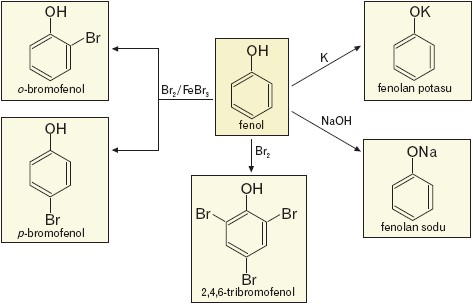
Przykładami innych fenoli są np. metylowe pochodne fenolu, czyli krezole:
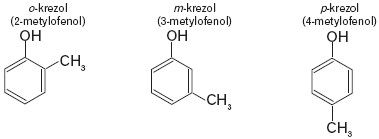
Fenole będące pochodnymi naftalenu to naftole.
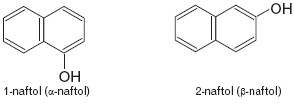
Fenole z 2 grupami –OH w cząsteczce to np.: