| stan hybrydyzacji orbitali walencyjnych atomów węgla | krotność wiązania pomiędzy atomami węgla | długość wiązania pojedynczego węgiel–węgiel | energia wiązania pojedynczego węgiel–węgiel |
| sp3 | wiązanie pojedyncze | 154 pm | 338 kJ/mol |
Cząsteczki alkanów zbudowane są z atomów węgla, których orbitale walencyjne są w stanie hybrydyzacji sp3. Atomy węgla połączone są ze sobą wyłącznie wiązaniami pojedynczymi σ. Długość wiązania pojedynczego węgiel-węgiel wynosi 154 pm,a energia wiązania 338 kJ/mol.
Cząsteczki alkanów nie są płaskie, a możliwość obrotu atomów lub grup atomów połączonych z sąsiednimi atomami węgla wokół wiązania σ powoduje, że istnieją różnorodne orientacje w przestrzeni określane mianem konformacji cząsteczki (dotyczy to stanu gazowego i ciekłego węglowodoru).
Rozważając cząsteczkę metanu, najprostszego alkanu i stosując teorię VSEPR do przewidywania rzeczywistego jej kształtu, stwierdzamy, że:

Skoro LH = 4, to:
- orbitale walencyjne atomu węgla są w stanie hybrydyzacji sp3.
- cząsteczka ma kształt tetraedru (brak wolnych par elektronowych na atomie węgla), czyli zgodny z przestrzennym rozmieszczeniem hybryd.
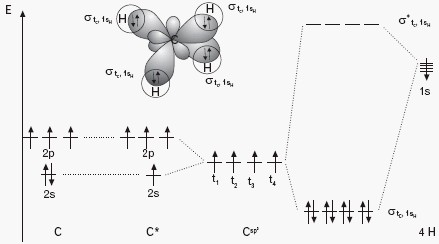
Poniżej przedstawiono diagram poziomów energetycznych dla cząsteczki metanu oraz schemat nakładania orbitali atomowych w cząsteczce metanu.
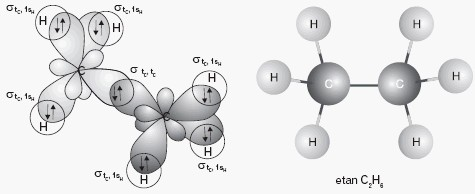
Schemat nakładania orbitali atomowych oraz model cząsteczki etanu przedstawiono poniżej.
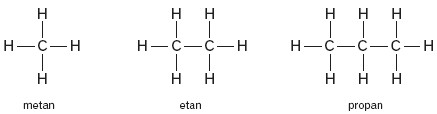
Alkany tworzą szereg homologiczny o wzorze ogólnym: CnH2n+2 (gdzie n oznacza liczbę atomów węgla w cząsteczce). Poszczególne człony szeregu zwane homologami różnią się o taki sam element strukturalny (–CH2–) lub jego krotność.
Wiązanie węgiel-wodór jest praktycznie niespolaryzowane (ΔE = 0,4), zatem cząsteczki alkanów są na ogół niepolarne. Niepolarne cząsteczki nie mogą utworzyć z cząsteczkami wody wiązań wodorowych, co jest warunkiem rozpuszczalności w wodzie. Alkany jako substancje hydrofobowe są praktycznie nierozpuszczalne w wodzie, a rozpuszczają się w rozpuszczalnikach organicznych. Właściwości fizyczne wybranych alkanów, w tym temperatury wrzenia (TW) i topnienia (TT), zestawiono w poniższej tabeli.
| węglowodór | TT [°C] | TW [°C] | właściwości fizyczne |
| metan CH4 |
–182,43 | –161,48 | bezbarwny, bezwonny gaz tworzący z powietrzem mieszaninę wybuchową, nierozpuszczalny w wodzie, rozpuszczalny w rozpuszczalnikach organicznych (eter, benzyna) |
| etan C2H6 |
–183,20 | –88,60 | bezbarwny, bezwonny, palny gaz słabo rozpuszczalny w wodzie, rozpuszczalny w rozpuszczalnikach organicznych (etanol) |
| n-butan C4H10 |
–138,30 | –0,55 | bezbarwny, palny gaz, słabo rozpuszczalny w wodzie, rozpuszczalny w alkoholu i eterze |
| n-heksan C6H14 |
–95,30 | 68,7 | bezbarwna, lotna, palna ciecz o zapachu benzyny, nierozpuszczalna w wodzie, rozpuszczalna w rozpuszczalnikach organicznych |
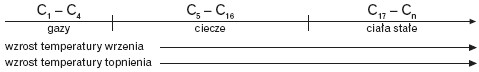
Homologi wykazują podobne właściwości chemiczne (szereg alkanów), a właściwości fizyczne stopniowo w tym szeregu zmieniają się ze wzrostem długości łańcucha węglowego w następujący sposób:
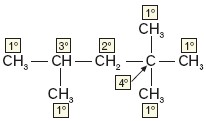
Rzędowość danego atomu węgla określona jest liczbą innych atomów węgla bezpośrednio z nim połączonych, np.: