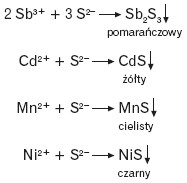Siarka pali się niebieskim płomieniem, a wydzielający się gaz ma nieprzyjemną, duszącą woń. Ma on właściwości bakteriobójcze oraz jest trujący. Powstający gaz to tlenek siarki(IV):
![]()
Gaz ten reaguje z wodą, tworząc słaby kwas siarkowy(IV).
![]()
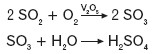
Utlenianie tlenku siarki(IV) w obecności katalizatora (np. V2O5) pozwala na otrzymanie tlenku siarki(VI). Ta biała substancja stała energicznie reaguje z wodą, tworząc kwas siarkowy(VI).
Kwas siarkowy(IV) jest nietrwały, istnieje tylko w roztworach wodnych.
Kwas siarkowy(VI) to gęsta, oleista, żrąca ciecz, bez zapachu. Jest higroskopijny.
| H2SO3 | H2SO4 |
| kwas słaby | kwas mocny, silnie utleniający |
| kwas nietrwały | kwas trwały |
|
|
|
| --- | z racji dwustopniowej dysocjacji tworzy dwa rodzaje soli: wodorosiarczany(VI) i siarczany(VI) |
Oleum to stężony kwas siarkowy(VI) z rozpuszczonym w nim nadmiarem tlenku siarki(VI).
Stężony kwas siarkowy(VI) zaliczany jest do kwasów silnie utleniających: utlenianie tylko metale, ale i niemetale.
![]()
Kwas siarkowy(VI) miesza się z wodą nieograniczenie, czemu towarzyszy wydzielanie ciepła.
Pamiętaj, że należy zawsze wlewać kwas do wody, aby nie nastąpił rozprysk kwasu i poparzenie. Stężony kwas siarkowy(VI) niszczy papier,skórę i bawełnę.
Pod wpływem stężonego kwasu siarkowego(VI) na przykład żelazo oraz ołów ulegają pasywacji.
Reakcją charakterystyczną na wykrycie jonów SO42– w roztworze jest reakcja z jonami Ba2+.
![]()
Siarkowodór to gaz o nieprzyjemnym zapachu zgniłych jaj. Jest trujący. Siarkowodór rozpuszczając się w wodzie tworzy kwas siarkowodorowy, który zaliczany jest do słabych kwasów.
Siarkowodór otrzymujemy w reakcjach:
- bezpośredniej syntezy

- działając mocnymi kwasami na określone związki
![]()
Większość siarczków metali to osady o charakterystycznych barwach. Strącanie osadów siarczków można traktować jako reakcję charakterystyczną dla jonów metali.